Bạn đã bao giờ gặp khó khăn trong việc giải các bài tập về công thức phân tử và hợp chất hữu cơ trong sách giáo trình Hóa 11 chưa? Đừng lo lắng nữa, bài viết này sẽ giúp bạn hiểu rõ hơn về cách giải các bài tập này một cách đơn giản và dễ dàng. Hãy cùng tìm hiểu ngay!
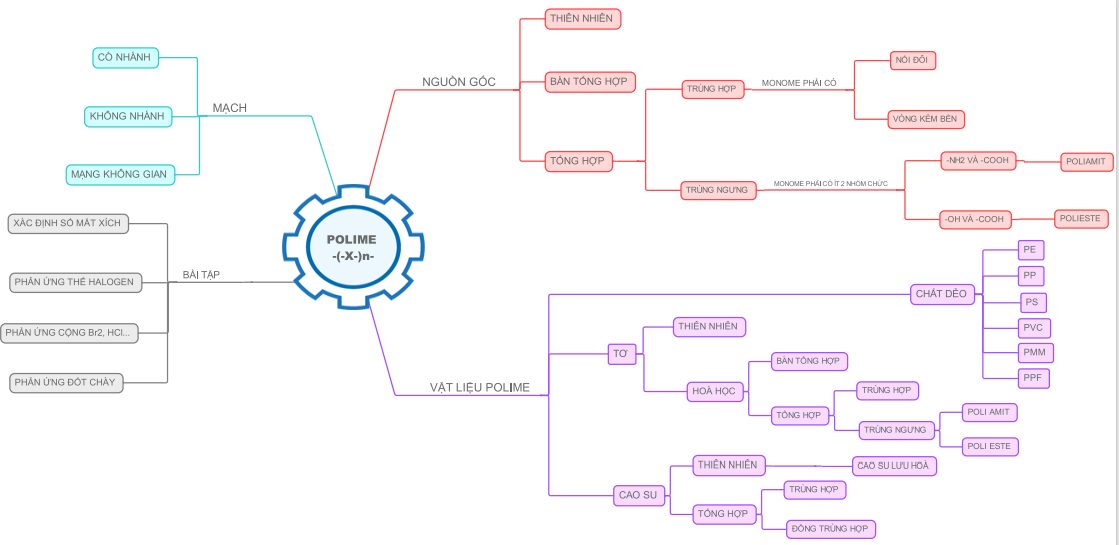
- Đại cương về polime – Những bí mật thú vị
- Hóa học 8 Bài 6: Đơn chất và Hợp chất – Phân tử: Tìm hiểu về các chất cơ bản
- Các từ khóa hữu ích cho việc học môn Địa lý thi tốt nghiệp THPT
- Đề cương ôn tập học kì 2 môn Hóa học lớp 9 – Chia sẻ tài liệu hữu ích
- Tuyển chọn 24 mã đề môn Hóa học thi tốt nghiệp THPT 2023
Công thức phân tử và công thức cấu tạo
Công thức phân tử cho biết tỉ lệ số nguyên tử của các nguyên tố trong phân tử. Nó giúp chúng ta biết được số nguyên tử của các nguyên tố trong phân tử cũng như cách thức liên kết giữa chúng.
Bạn đang xem: Cách giải bài 1, 2, 3, 4, 5, 6 trang 95 SGK Hóa 11: Công thức phân tử – Hợp chất hữu cơ
.png)
Tính khối lượng mol phân tử
Để tính khối lượng mol phân tử của một chất hữu cơ, ta dựa vào tỉ khối hơi của chất đó. Từ đó, ta có thể xác định được công thức phân tử và phân biệt được các hiđrocacbon và dẫn xuất của chúng.
Hướng dẫn giải các bài tập trang 95
Bài 1: Tính khối lượng mol phân tử của chất A
Ta có:
- Tỉ lệ khối hơi của chất A so với không khí là 2,07.
- Thể tích hơi của 3,3 gam chất khí X bằng thể tích của 1,76 gam khí oxi.
Áp dụng công thức tính khối lượng mol phân tử, ta có kết quả là 60,0 (g/mol).
Bài 2: Lập công thức phân tử của limonen
Limonen là một chất có mùi thơm dịu được tách từ tinh dầu chanh. Phân tích nguyên tử cho thấy, limonen gồm hai nguyên tố C và H, với tỉ lệ khối lượng của C là 88,235%. Từ tỉ khối hơi gần bằng 4,69, ta lập được công thức phân tử của limonen là C10H16.
Bài 3: Xác định công thức phân tử của chất A
Chất A chứa các nguyên tử C, H, O. Thông qua việc đốt cháy hoàn toàn 0,3 gam chất A, ta thu được 0,44 gam khí cacbonic và 0,18 gam nước. Bằng cách tính số mol, ta xác định được công thức phân tử của chất A là C2H4O2.
Bài 4: Lập công thức đơn giản nhất và công thức phân tử của anetol
Anetol là một chất thơm được tách từ tinh dầu hồi. Phân tích nguyên tử cho thấy, chất này gồm C, H, O với %C là 81,08% và %H là 8,1%. Từ đó, ta lập được công thức phân tử của anetol là C10H12O.
Bài 5: Xác định hợp chất từ phần trăm khối lượng cacbon, hiđro và oxi
Một hợp chất X có %C là 54,54%, %H là 9,1% và %O là 36,36%. Khối lượng mol phân tử của X là 88 g/mol. Từ các phần trăm khối lượng và khối lượng mol phân tử, ta xác định được công thức phân tử của X là C4H8O2.
Bài 6: Xác định công thức phân tử của hợp chất Z
Hợp chất Z có công thức đơn giản nhất là CH3O và tỉ khối hơi so với hiđro là 31. Từ đó, ta lập công thức phân tử của Z là C2H6O2.
Đây là cách giải các bài tập trang 95 SGK Hóa 11 về công thức phân tử và hợp chất hữu cơ. Hy vọng rằng bài viết này sẽ giúp bạn hiểu rõ hơn về chủ đề này và thành công trong việc giải các bài tập tương tự. Nếu bạn cần thêm thông tin, hãy ghé thăm Izumi.Edu.VN – trang web chuyên về giáo dục và đào tạo.
Nguồn: https://izumi.edu.vn/
Danh mục: Tài liệu hóa