Trong bài học hóa học, chúng ta sẽ tìm hiểu về dẫn xuất halogen của hidrocacbon. Mặc dù ít được nhắc đến, nhưng chúng là những hợp chất trung gian rất quan trọng giữa hidrocacbon và các hợp chất hữu cơ khác. Vậy dẫn xuất halogen có những đặc điểm vật lý và hóa học nào? Chúng được phân loại ra sao? Cùng tìm hiểu nhé!
- 10 Bài Nghị Luận Xã Hội về Ước Mơ Chọn Lọc Hay Nhất
- Câu 1, 2, 3 trang 49 Vở bài tập Toán 5 tập 2: Những bí mật số thời gian và lịch sử!
- Phương pháp điện phân muối NaCl: Tìm hiểu và lựa chọn thiết bị phù hợp
- Công nghệ hàng không của tương lai: Thiết kế và ưu điểm
- Phương Trình Điện Li của Na2S: Những Bí Mật Được Tiết Lộ
Khái niệm, phân loại, đồng phân và danh pháp của dẫn xuất halogen
Khái niệm
Dẫn xuất halogen của hidrocacbon là sản phẩm chúng ta thu được khi thay thế một hay nhiều nguyên tử hiđro trong phân tử hidrocacbon bằng một hay nhiều nguyên tử halogen.
Bạn đang xem: Dẫn xuất halogen của hidrocacbon – Học tốt hóa 11 cùng Toppy
Phân loại
Có nhiều cách để phân loại dẫn xuất halogen. Cụ thể:
-
Phân loại theo nguyên tố: dẫn xuất Clo, dẫn xuất Brom, dẫn xuất Flo, dẫn xuất Iot và dẫn xuất chứa đồng thời một vài halogen.
-
Phân loại theo cấu tạo của gốc hidrocacbon gồm có:
- Dẫn xuất hidrocacbon no: CH2FCl, CH2Cl-CH2Cl, CH3-CHBr-CH3, (CH3)3C-ICH2FCl, CH2Cl-CH2Cl, CH3-CHBr-CH3, (CH3)3C-I.
- Dẫn xuất halogen không no: CF2=CF2, CH2=CH-Cl, CH2=CHCH2-BrCF2=CF2, CH2=CH-Cl, CH2=CHCH2-Br.
- Dẫn xuất halogen thơm: C6H5F, C6H5CH2-Cl, p-CH3C6H4Br, C6H5IC6H5F, C6H5CH2-Cl, p-CH3C6H4Br,C6H5I.
-
Phân loại theo bậc của dẫn xuất halogen bằng bậc của nguyên tử cacbon liên kết với nguyên tử halogen.
Đồng phân và danh pháp
Đồng phân
Dẫn xuất halogen sẽ có đồng phân mạch cacbon giống như hiđrocacbon. Đồng thời, chúng cũng đồng phân về vị trí nhóm chức.
Tên thông thường
Một số ít các dẫn xuất hidrocacbon được gọi theo tên thông thường, ví dụ như: CHCl3 (clorofom), CHBr3 (bromofrom), CHI3 (iođofom).
Tên gốc – chức
Tên của các dẫn xuất halogen đơn giản được cấu tạo từ tên gốc hidrocacbon + halogenua, ví dụ: metylen clorua, vinyl florua, anlyl clorua, benzyl bromua.
Tên thay thế
Trong một số trường hợp, dẫn xuất halogen sẽ được gọi theo tên thay thế. Các nguyên tử halogen sẽ được coi là những nhóm thế được đính vào mạch chính của hiđrocacbon, ví dụ như:
- CH3CH2CH2X (X = F, Cl, Br, I) được gọi là propyl florua, propyl clorua, propyl bromua, propyl iodua.
Tính chất vật lí
Tính chất vật lí của dẫn xuất halogen như sau:
- Các dẫn xuất monohalogen có phân tử khối nhỏ như CH3F, CH3Cl, CH3Br là chất khí ở điều kiện bình thường.
- Các dẫn xuất halogen có phân tử khối lớn hơn sẽ là chất lỏng và nặng hơn nước, ví dụ như CH3I, CH2Cl2, CHCl3, CCl4, C2H4Cl2, C6H5Br.
- Những dẫn xuất polihalogen có phân tử khối lớn hơn nữa sẽ tồn tại ở dạng chất rắn, ví dụ như CHI3, C6H6Cl6.
- Dẫn xuất halogen hầu hết không tan trong nước, nhưng tan tốt trong các dung môi không phân cực như hiđrocacbon, ete, vv.
- Nhiều dẫn xuất halogen cũng có hoạt tính sinh học cao, ví dụ như CHCl3 có thể được sử dụng để gây mê, C6H6Cl6 có công dụng là diệt sâu bọ.
Tính chất hóa học của dẫn xuất halogen
Phản ứng thế nguyên tử halogen bằng nhóm -OH
Trong một thí nghiệm, các nhà hóa học đã nghiên cứu phản ứng thế nguyên tử halogen bằng nhóm -OH trong các dẫn xuất halogen của hidrocacbon. Khi tiến hành thí nghiệm với 33 chất lỏng đại diện cho các nhóm ankyl halogenua, anlyl halogenua và phenyl halogenua, kết quả như sau:
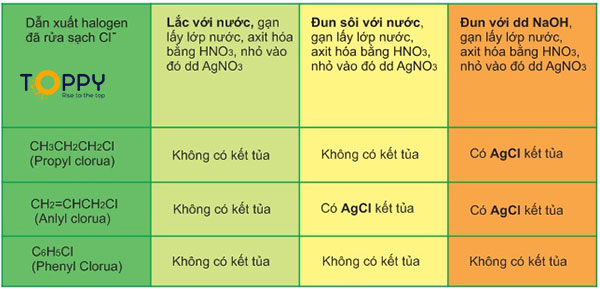
Từ bảng trên, ta có thể thấy:
- Dẫn xuất loại ankyl halogenua không phản ứng với nước ở điều kiện thường, nhưng sẽ bị thủy phân khi đun nóng cùng với dung dịch kiềm để tạo thành ancol.
- Dẫn xuất loại ankyl halogenua sẽ bị thủy phân ngay khi đun sôi cùng với nước.
- Dẫn xuất loại phenyl halogenua sẽ không phản ứng với dung dịch kiềm trong điều kiện thường, chỉ tham gia phản ứng trong điều kiện nhiệt độ và áp suất cao (300 độ C và 200atm).
Phản ứng tách hiđro halogenua
Khi đun sôi dung dịch chứa C2H5Br và KOH trong C2H5OH, ta có thể nhận biết khí sinh ra bằng nước brom.
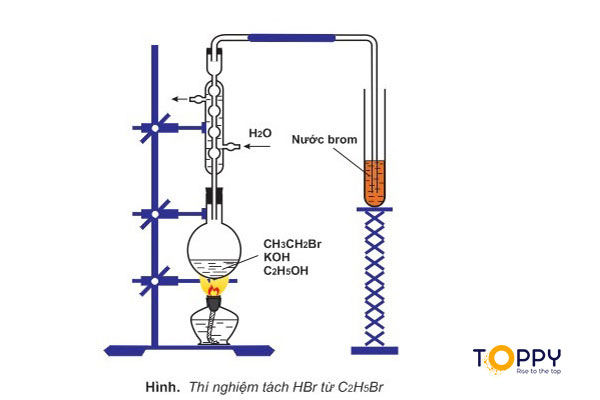
Khí sinh ra sau phản ứng sẽ làm mất màu nước brom và tạo thành những giọt chất lỏng không tan trong nước (C2H4Br2). Khí đó chính là CH2=CH2 (etilen). Đây chính là phản ứng tách HBr ra khỏi C2H5Br.
Phản ứng với magie
Trong thí nghiệm, cho bột magie vào đietyl ete khan và khuấy mạnh hỗn hợp. Quan sát phản ứng, ta thấy bột magie hoàn toàn tan hết.

Etyl magie bromua có liên kết trực tiếp giữa cacbon và kim loại (C−Mg), chúng thuộc loại hợp chất cơ kim (hữu cơ – kim loại). Liên kết C−Mg là trung tâm phản ứng. Hợp chất cơ magie tác dụng nhanh với các chất linh động như nước, ancol, vv.
Ứng dụng
Dẫn xuất polihalogen được sử dụng làm dung môi, nguyên liệu cho tổng hợp hữu cơ, chất gây mê trong phẫu thuật, diệt sâu bọ, thuốc diệt cỏ, vv.
Trên đây là những thông tin cơ bản về dẫn xuất halogen, tính chất vật lý và hóa học của chúng. Để tìm hiểu thêm về các kiến thức hóa học khác, bạn có thể truy cập vào địa chỉ: Izumi.Edu.VN
Nguồn: https://izumi.edu.vn/
Danh mục: Kiến thức chung





